1 病毒间相互作用
1.1 相互促进作用
1.2 相互抑制作用
1.3 免疫逃逸作用
2 多病毒耦合传播模型
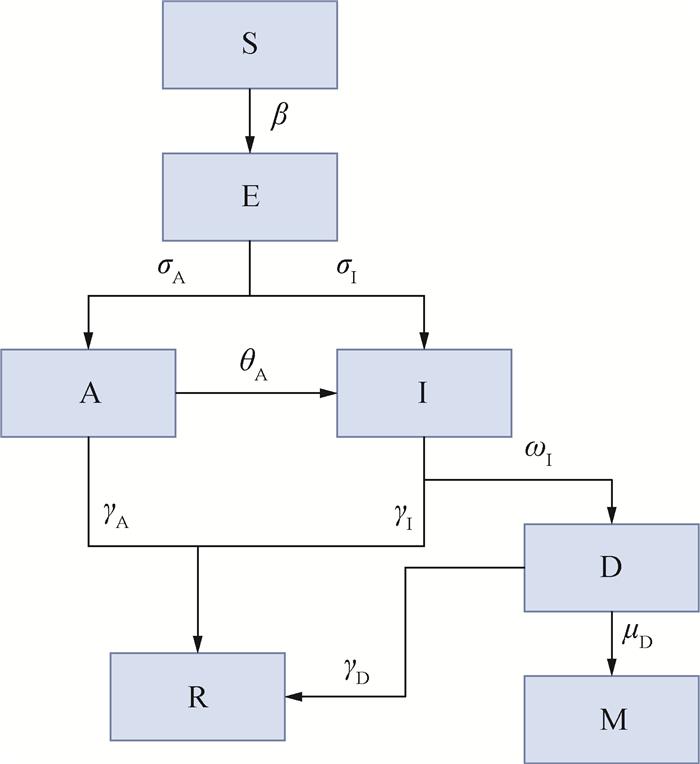
2.1 SEAIDRM模型
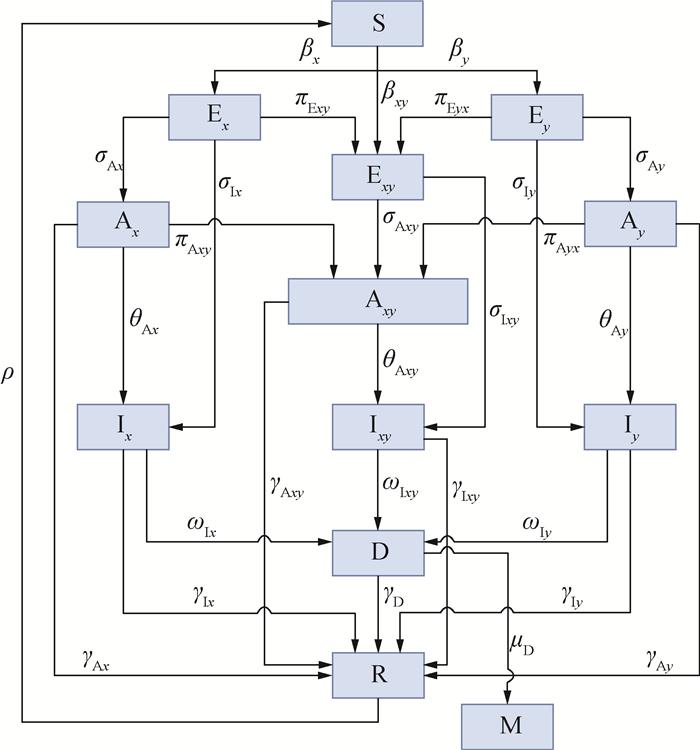
2.2 多病毒耦合传播模型
表 1 多病毒耦合动力学模型参数表 |
| 参数 | 含义 |
| βx | S感染x变成Ex的概率 |
| βy | S感染y变成Ey的概率 |
| βxy | S感染x、y变成Exy的概率 |
| σAx | Ex转变为Ax的概率 |
| σIx | Ex转变为Ix的概率 |
| πExy | Ex转变为Exy的概率 |
| σAy | Ey转变为Ay的概率 |
| σIy | Ey转变为Iy的概率 |
| πEyx | Ey转变为Exy的概率 |
| σAxy | Exy转变为Axy的概率 |
| σIxy | Exy转变为Ixy的概率 |
| γAx | Ax转变为R的概率 |
| θAx | Ax转变为Ix的概率 |
| πAxy | Ax转变为Axy的概率 |
| γAy | Ay转变为R的概率 |
| θAy | Ay转变为Iy的概率 |
| πAyx | Ay转变为Axy的概率 |
| γAxy | Axy转变为R的概率 |
| θAxy | Axy转变为Ixy的概率 |
| γIx | Ix转变为R的概率 |
| ωIx | Ix转变为D的概率 |
| γIy | Iy转变为R的概率 |
| ωIy | Iy转变为D的概率 |
| γIxy | Ixy转变为R的概率 |
| ωIxy | Ixy转变为D的概率 |
| γD | D转变为R的概率 |
| μD | D转变为M的概率 |
| ρ | R再次转变为S的概率 |
2.3 病毒间相互作用对耦合模型的影响
3 模拟实验与结果分析
表 2 x和y耦合传播模型关键参数 |
| 参数 | 取值 | 依据说明 |
| βx | 0.25 | 病毒性呼吸道传染病的基本再生数为1.3~5.0,传染期为3~21 d,βx=基本再生数/(传染期/d),取0.25 |
| βy | 0.18 | 病毒性呼吸道传染病的基本再生数为1.3~5.0,传染期为3~21 d,βy=基本再生数/(传染期/d),取0.18 |
| σAx | 0.20 | 病毒性呼吸道传染病的潜伏期约为1~14 d,σAx=1/(潜伏期/d),取0.20 |
| σIx | 0.10 | 病毒性呼吸道传染病的潜伏期约为1~14 d,σIy=1 /(潜伏期/d),取0.10 |
| σAy | 0.12 | 病毒性呼吸道传染病的潜伏期约为1~14 d,σAy=1/(潜伏期/d),取0.12 |
| σIy | 0.08 | 病毒性呼吸道传染病的潜伏期约为1~14 d,σIy=1/(潜伏期/d),取0.08 |
| γAx | 0.08 | 病毒性呼吸道传染病的无症状感染者平均自愈时间约为3~14 d,γAx=1/(无症状感染者平均自愈时间/d),取0.08 |
| θAx | 0.15 | 病毒性呼吸道传染病的无症状感染者发展为有症状感染者的概率取10%~20% |
| γAy | 0.12 | 病毒性呼吸道传染病的无症状感染者平均自愈时间约为3~14 d,γAy=1/(无症状感染者平均自愈时间/d),取0.12 |
| θAy | 0.10 | 病毒性呼吸道传染病的无症状感染者发展为有症状感染者的概率取10%~20% |
| γIx | 0.07 | 病毒性呼吸道传染病的有症状感染者平均自愈时间约为3~21 d,γIx=1/(有症状感染者平均自愈时间/d),取0.07 |
| ωIx | 0.05 | 病毒性呼吸道传染病的隔离率取5% |
| γIy | 0.08 | 病毒性呼吸道传染病的有症状感染者平均自愈时间约为3~21 d,γIy=1/(有症状感染者平均自愈时间/d),取0.08 |
| ωIy | 0.05 | 病毒性呼吸道传染病的隔离率取5% |
| γD | 0.07 | 隔离后平均恢复时间约为10~21 d,γD=1 / (隔离后平均恢复时间/d),取0.07 |
3.1 模拟场景设置
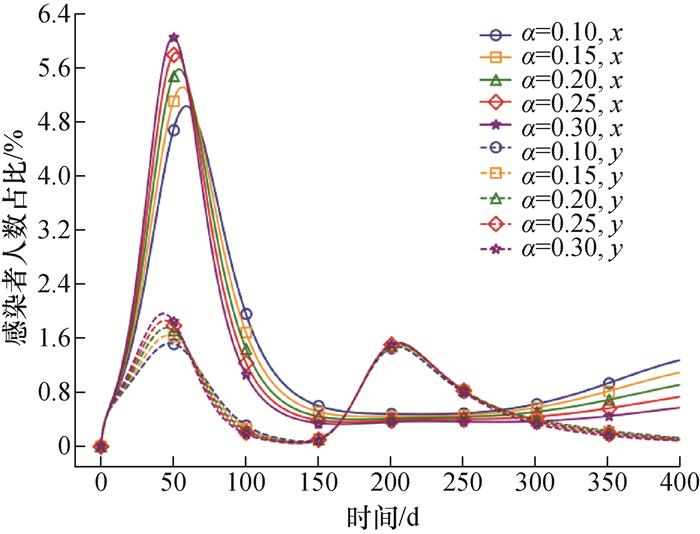
3.2 相互促进强度对多病毒耦合传播影响模拟
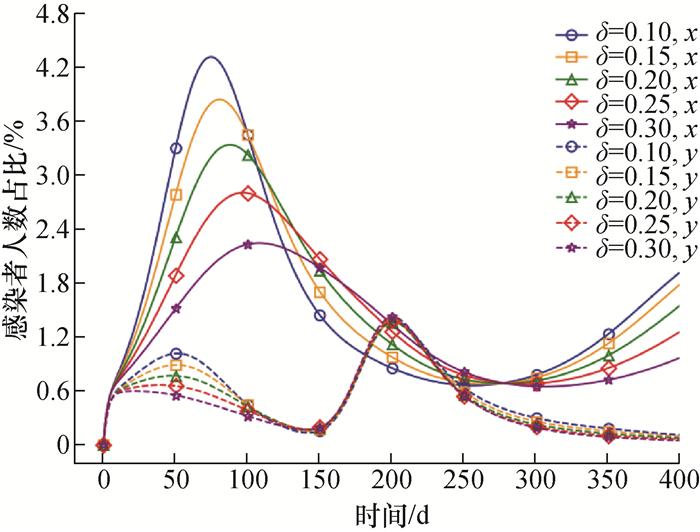
3.3 相互抑制强度对多病毒耦合传播影响模拟
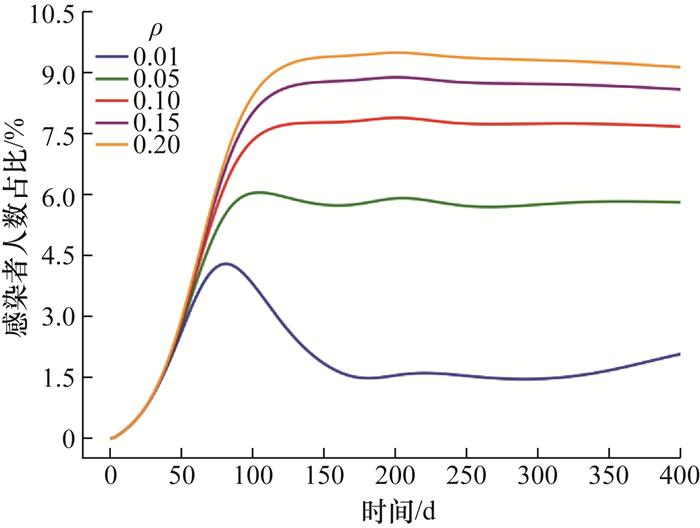
3.4 免疫逃逸作用对多病毒耦合传播影响模拟
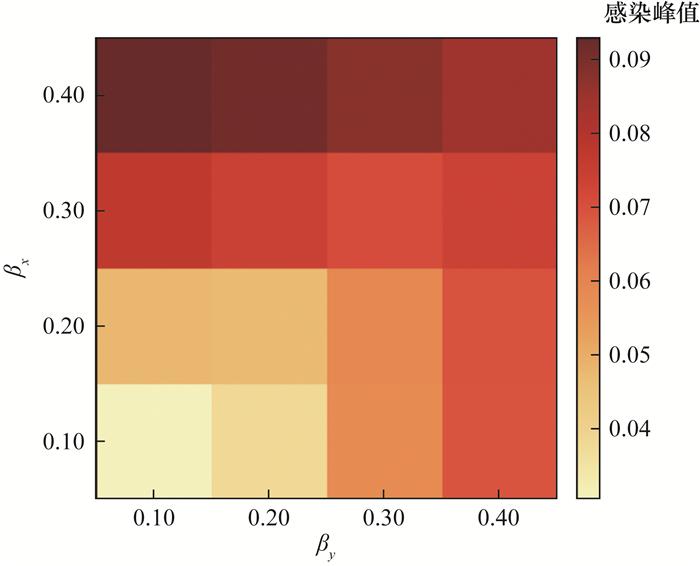
3.5 传播率参数对感染峰值的影响分析
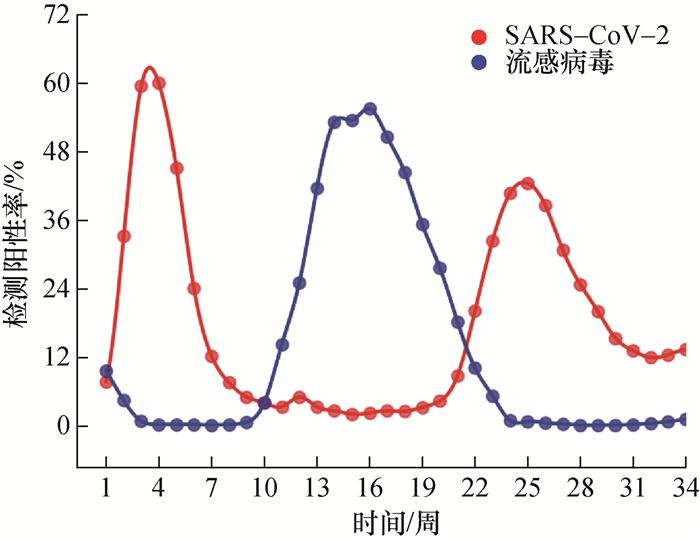
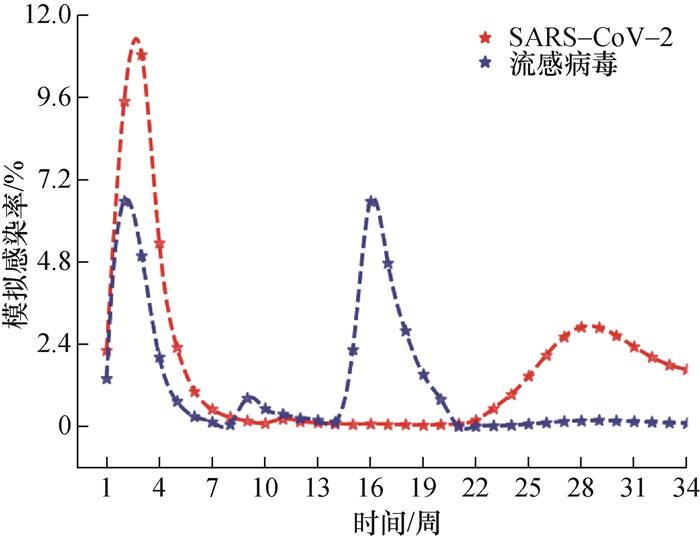
4 实例验证
4.1 数据说明
表 3 SARS-CoV-2和流感病毒耦合传播模型关键参数 |
| 参数 | 取值 | 依据说明 |
| βx | 0.35 | SARS-CoV-2的基本再生数为2.5,传染期为7 d,βx=基本再生数/(传染期/d),取0.35 |
| βy | 0.20 | 流感病毒的基本再生数为1.4,传染期为7 d,βy=基本再生数/(传染期/d),取0.20 |
| σAx | 0.20 | SARS-CoV-2潜伏期约为1~14 d,σAx=1/(潜伏期/d),取0.20 |
| σIx | 0.14 | SARS-CoV-2潜伏期约为1~14 d,σIx= 1/(潜伏期/d),取0.14 |
| σAy | 0.30 | 流感病毒潜伏期约为1~4 d,σAy=1/(潜伏期/d),取0.30 |
| σIy | 0.25 | 流感病毒潜伏期约为1~4 d,σIy=1/(潜伏期/d),取0.25 |
| γAx | 0.07 | SARS-CoV-2无症状感染者平均自愈时间约为7~14 d,γAx=1/(无症状感染者平均自愈时间/d),取0.07 |
| θAx | 0.15 | SARS-CoV-2无症状感染者发展为有症状感染者的概率取10%~20% |
| γAy | 0.20 | 流感病毒无症状感染者平均自愈时间约为3~5 d,γAy=1/(无症状感染者平均自愈时间/d),取0.20 |
| θAy | 0.15 | 流感病毒无症状感染者发展为有症状感染者的概率取10%~20% |
| γIx | 0.05 | SARS-CoV-2有症状感染者平均自愈时间约为14~21 d,γIx=1/(有症状感染者平均自愈时间/d),取0.05 |
| ωIx | 0.10 | SARS-CoV-2隔离率取10% |
| γIy | 0.14 | 流感病毒有症状感染者平均自愈时间约为3~7 d,γIy=1/(有症状感染者平均自愈时间/d),取0.14 |
| ωIy | 0.02 | 流感病毒隔离率取2% |
| γD | 0.07 | 隔离后平均恢复时间约为15 d,γD=1/(隔离后平均恢复时间/d),取0.07 |
备注:x代表SARS-CoV-2;y代表流感病毒。 |